Bạn đã từng nghe đến khái niệm “Bảng Tính Tan” trong môn hóa học, đúng không? Đó là một trong những kiến thức quan trọng từ lớp 8 đến lớp 12. Tuy nhiên, việc ghi nhớ kiến thức này không phải là điều dễ dàng. Vậy hãy cùng tìm hiểu chi tiết về bảng tính tan và cách học hiệu quả nhé!
I. Bảng Tính Tan Là Gì?
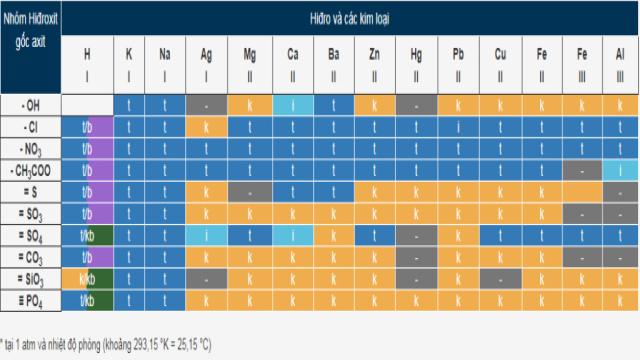
Bảng tính tan bao gồm các hàng và cột, trong đó cột đại diện cho các cation kim loại, còn hàng đại diện cho các anion gốc axit hoặc OH-. Nhờ bảng tính tan, chúng ta có thể xác định trạng thái của một chất tại một ô cụ thể.
II. Chất Tan và Chất Không Tan
Trong nước, có nhiều chất tan và không tan, có chất tan ít và chất tan nhiều. Ví dụ, hầu hết axit đều tan trong nước, trừ axit silicic. Còn đối với bazo, phần lớn các bazo không tan trong nước, trừ một số như KOH và NaOH. Về muối, các muối natri, kali đều tan, nhưng các muối cacbonat thường không tan.
III. Độ Tan Của Một Chất Trong Nước
Độ tan của một chất trong nước được định nghĩa là số gam chất đó tan trong 100 gam nước để tạo thành dung dịch bão hoà ở một nhiệt độ nhất định. Độ tan của một chất phụ thuộc vào nhiệt độ và áp suất. Với chất rắn trong nước, độ tan sẽ tăng khi nhiệt độ tăng và giảm khi nhiệt độ giảm. Còn với chất khí trong nước, độ tan sẽ tăng khi giảm nhiệt độ và tăng áp suất.
IV. Đặc Tính Tan Trong Nước Của Axit, Bazo và Muối
Mỗi hợp chất đều có đặc tính tan khác nhau. Ví dụ, hầu hết các axit đều tan trong nước, trừ axit silicic. Các bazo hầu như không tan trong nước, trừ một số như KOH và NaOH. Với muối, muối kali, natri đều tan, muối nitrat đều tan, nhưng muối clorua, sunfat thường tan, còn muối cacbonat thường không tan.
V. Ý Nghĩa Bảng Tính Tan
Bảng tính tan cho ta biết tính tan của các chất trong nước, từ đó ta có thể làm các bài nhận biết và các bài toán có liên quan. Ví dụ, nhận biết dung dịch muối sắt (III) bằng dung dịch NaOH để tạo thành kết tủa màu nâu đỏ Fe(OH)3.
VI. Bảng Tính Tan Hóa Học
Bảng tính tan là nội dung quan trọng trong giải các bài toán hóa học. Dưới đây là bảng tính tan hóa học ở nhiệt độ phòng, áp suất 1 atm:
| | t | k | b | i | - |
|----|----|----|----|----|----|
| t | t | k | b | i | - |
| k | t | k | b | i | - |
| b | t | k | b | i | - |
| i | t | k | b | i | - |
| - | - | - | - | - | - |VII. Bảng Tính Tan Của Muối và Hiđroxit
Bạn có thể xem bảng tính tan của muối và hiđroxit trong hình ảnh dưới đây:
VIII. Cách Ghi Nhớ Bảng Tính Tan
Để ghi nhớ bảng tính tan, có một số quy tắc rút gọn mà bạn có thể áp dụng. Ví dụ, muối có gốc halogen như Cl, Br, F thường tan trong nước, nhưng muối có gốc silicat, sunfit, cacbonat, sunfua thường không tan hoặc khó tan trong nước. Các kim loại kiềm như K, Na, Li sau khi kết hợp thành muối đều tan trong nước.
IX. Muối Nào Tan Trong Nước và Muối Nào Không Tan?
Muối có gốc axit, nitrat, axetat thường tan trong nước, trong khi muối gốc photphat, sunfua, cacbonat thường không tan. Có một số muối không tồn tại hoặc bị phân huỷ ngay trong nước.
X. Màu Sắc Của Một Số Hiđroxit Không Tan
Các hiđroxit không tan có màu sắc khác nhau. Ví dụ, Cu(OH)2 có kết tủa xanh lam, Fe(OH)2 có kết tủa lục nhạt, Fe(OH)3 có kết tủa nâu đỏ, Mg(OH)2 có kết tủa trắng không tan trong kiềm dư, Al(OH)3, Zn(OH)2, Pb(OH)2, Sn(OH)2 có kết tủa trắng tan trong kiềm dư.
XI. Mẹo Nhớ Bảng Tính Tan Qua Thơ
Có một thức thuật thú vị để ghi nhớ bảng tính tan: làm thơ! Những câu thơ ngắn và dễ nhớ sẽ giúp bạn nhớ lâu kiến thức về tính tan của các chất trong nước.
Đó là những bí mật bên trong bảng tính tan. Hy vọng rằng thông qua bài viết này, bạn đã có cái nhìn tổng quan về bảng tính tan và cách học hiệu quả. Hãy tiếp tục đồng hành cùng PRAIM trong hành trình khám phá kiến thức hóa học nhé!
Chào mừng bạn đến với PRAIM, - nền tảng thông tin, hướng dẫn và kiến thức toàn diện hàng đầu! Chúng tôi cam kết mang đến cho bạn một trải nghiệm sâu sắc và tuyệt vời về kiến thức và cuộc sống. Với Praim, bạn sẽ luôn được cập nhật với những xu hướng, tin tức và kiến thức mới nhất.